*Capturem Extracellular Vesicle Isolation Kit 제품은 2022년 8월 종매되었습니다.
질병 치료를 위한 EV (e.g. exosome)의 활용
Exosome과 같은 extracellular vesicles (EV)는 크기는 작지만, 생리 반응 (e.g. 면역 반응, 신경 기능, 줄기 세포 유지 기능)과 질병 병리 (e.g. 암, 간 질환)에 중요한 역할을 한다. EV는 세포 간 교류 과정에서
분비 및 흡수되면서, 단백질이나 RNA를 포함한 다양한 물질을 전달한다. EV가 이러한 세포 교류과정을 진행하지 못하면 다양한 질병이 유발될 수 있어, 이에 대한 관심이 집중 되고 있다.
EV가 인간의 건강과 발달에 대해 중요한 역할을 할 수 있다는 가능성 확인을 위해, 연구자들은 기존의 초원심분리를 이용하지 않고 EV를 추출하는 방법을 찾고자 했다. 초원심분리를 이용한 방법은
그동안 가장 많이 사용되는 방법이었으나, 특수한 장비가 필요하고, 시간이 많이 소요되는 반면, 얻을 수 있는 EV 수율은 낮고 손상되는 경우가 있었다.
최근, Stanford University Medical Center의 연구원들은 폐혈관 내 고혈압을 유발하는 폐동맥 고혈압 (pulmonary arterial hypertension, PAH)의 근본적인 원인에 대해 확인하고자 했고,
이 연구에서 Yuan
et al. 는 해당 혈관을 둘러싸는 세포의 exosome으로부터 이를 해결하기 위한 실마리를 찾았다.
A broken repair mechanism
혈관주위세포 (Pericyte)는 몸 전체의 모세혈관을 둘러싸는 특수한 벽화세포 (mural cell)로, 인간의 모든 혈관 조직의 성숙과 기능 유지에 중요한 역할을 한다. 연구자들은 PAH로 인해 폐에서의 미세혈관 내 혈관주위세포가 감소한 것을 확인하였으며, 폐 혈관주위세포와 미세혈관 간의 메커니즘을 조사하고자 했다.
정상 세포와 PAH pulmonary microvascular endothelial cells (PMVECs)에서 신생 미세 혈관 안정화에 필수 과정인 혈관주위세포의 작용을 확인하였다. 정상의 폐 혈관주위세포와 PMVECs를 공배양 했을 때는 혈관 생성이 명확하게 확인된 반면, PAH PMVECs를 동일한 조건에서 공배양 했을 때는 혈관 생성을 확인하지 못하였다.
연구자들은 선행 연구에서 PMVECs 주위로 Wnt/planar cell polarity (PCP) 신호 전달 경로를 통해 혈관주위세포를 모으는데 중요한 역할을 하고 있음을 확인하였다. 정상 PMVECs와 PAH PMVECs 모두에서 잘 특성화된 Wnt ligand의 발현을 확인했으며, 정상의 경우에는 PMVECs만 배양했을 때보다 혈관주위세포와 공배양 했을 때 Wnt5a의 발현이 월등하게 증가하는 것이 확인되었다. 반면, PAH PMVECs에서는 이러한 반응이 나타나지 않고, 세포 용해물을 이용해 Western blot을 진행했을 때에도 관찰되지 않았다. 이는 정상 PMVECs에서 siRNA를 이용해 Wnt5a를 knockdown 시켰을 때 결과와 유사하였다.
A failure to communicate
Wnt는 exosome이 운반하는 물질 중 하나로, 세포 간 이동하며 생물학적 활성을 유지할 수 있어 거리가 먼 세포 사이에서도 영향을 미칠 수 있다 (Luga
et al. 2012; Zhang
et al. 2014). Yuan
et al. 는 PMVEC 내 Wnt5a를 염색하여, exosome이 만들어지는 것을 확인하였다. 정상 PMVECs만 배양했을 때에는 퍼져있는 염색 상을 보였으나, 혈관주위세포와 공배양 했을 때에는 세포막 근처에 과도하게 모여 발현하는 것을 확인하였다. 반면, PAH PMVECs에서는 일반적으로 낮은 Wnt5a 발현을 보였으며, 혈관주위세포와 공배양 했을 때에도 유의한 변화는 확인되지 않았다.
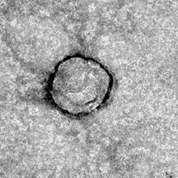
이 결과를 바탕으로, 연구자들은 PMVECs로부터 exosome을 분리하여 Wnt5a 발현을 확인하고자 했다. 초원심분리를 이용한 Exosome 분리는 가장 많이 사용되는 방법이지만 그 한계로 인해 ExoTIC 기술을 개발했고, 더 적은 양의 체액으로부터 filter membrane을 이용해 대량의 exosome을 분리할 수 있었다. 이렇게 추출한 exosome을 이용하여 PMVECs의 단일 배양, 공배양 처리하여 실험을 진행했다. 특히,
Capturem™ EV spin columns으로부터 분리된 exosome은 TEM을 이용해 선명한 이미지로 관찰할 수 있었다 (그림1).
ExoTIC 방법으로 정제된 exosome을 처리하여 함께 배양했을 때, 혈관주위세포와 함께 배양한 정상세포에서는 exosome과 Wnt5a 발현이 증가하였음을 Western blot과 면역형광염색을 통해 확인 하였으나, PAH PMVECs에서는 변화가 없었다.
Wnt5a를 포함하는 exosome에서 생물학적 활성을 유지하는지 확인하기 위해 후속 실험을 진행하였고, 실제로 정상 PMVECs로부터 추출한 exosome을 PAH PMVECs에 첨가하여 공배양 했을 때 혈관주위세포 이동 (recruitment)이 증가했다. 동일한 방법으로 Wnt5a가 knockdown된 PMVECs 유래의 exosome을 처리했을 때에는 혈관주위세포 이동 (recruitment)이 감소하였다.
이 실험을 통해, 세포 간 교류가 감소했을 때 정상 혈관을 수복하고 유지하기 위해 exosome이 Wnt5a를 전달 함으로써 세포의 정상 기능 유지에 기여한다는 것을 확인하였다.
[원문] Small but mighty: gaining insight into pulmonary arterial hypertension with purified exosomes
[참고문헌]
- Luga, V.,
et al. Exosomes mediate stromal mobilization of autocrine Wnt-PCP signaling in breast cancer cell migration.
Cell 151, 1542-1556 (2012).
- Zhang, L. and Wrana, J. L. The emerging role of exosomes in Wnt secretion and transport.
Curr. Opin. Genet. Dev. 27, 14-19 (2014).
- Yuan, K.,
et al. Loss of endothelium-derived Wnt5a is associated with reduced pericyte recruitment and small vessel loss in pulmonary arterial hypertension.
Circulation 139, 1710-1724 (2019).