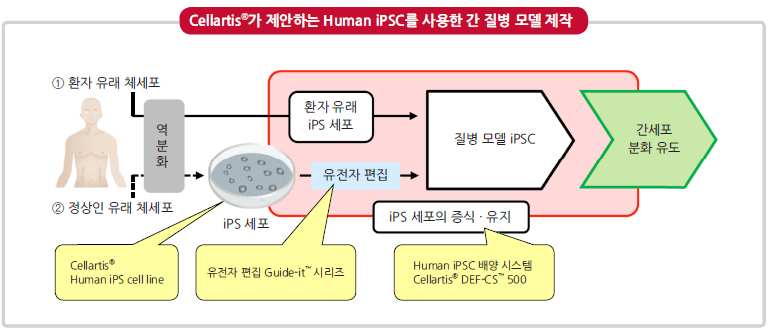
Human iPSC를 사용한 질병 모델 제작과 병태 해석 연구를 위한
Cellartis® iPS Cell to Hepatocyte Differentiation System의 적용사례를 확인하세요.
- 환자 유래 iPSC 또는 유전자 편집된 iPSC로부터 최적화 과정 없이 간세포로 고순도 분화 (90% 이상)
- Cellartis의 독자적인 기술로 iPSC 초보자도 높은 분화 효율과 안정적인 실험 결과 도출
- 분화 유도에 필요한 배지를 모두 포함한 All-in-One kit
1. 선천성 간 섬유증 (Congential hepathic fibrosis) 모델 개발과 병태 연구
Department of Gastroenterology and Hepatology, Tokyo Medical and Dental University (TMDU)
PhD. Sei Kakinuma
Cellartis® iPS Cell to Hepatocyte Differentiation System (Code Y30055)을 이용한 선천성 간 섬유증 모델 제작과 병태 규명의 연구 성과가 Journal of Hepatology에 게재되었습니다.
[논문명]
Tsunoda, Tomoyuki, et al. "Loss of fibrocystin promotes interleukin-8-dependent proliferation and CTGF production of biliary epithelium." Journal of hepatology 71.1 (2019): 143-152.

선천성 간섬유증은 태아기에 시작되는 담관 형성의 이상과 간섬유화를 일으키는 유전성 간질환이다. 소아기에 간이식을 필요로 할 수 있는 난치성 질환으로, 신규 치료법을 개발하기 위해
질병모델 확립이 필요한 상태이다. 지금까지는 해당 질환의 마우스 모델을 이용한 연구가 이루어졌지만, 마우스 모델과 실제 환자의 병태에는 격차가 큰 것이 한계였다. 연구진은 Human iPSC에서
본 질환을 재현 및 해석할 수 있는 질병 모델을 제작하여, 담관 세포가 생성하는 IL-8이 본 질환에서 볼 수 있는 담관의 이상과 간섬유화의 진행에 중요한 역할을 수행함을 발견하였다.
또한, Human iPSC 질병 모델에서 얻은 결과는 선천성 간섬유증을 가진 실제 환자에서도 관찰 할 수 있었다. 따라서, 본 연구를 통해 Human iPSC를 이용한 질병 모델을 개발함으로써,
처음으로 선천성 간섬유증의 병태에 대해 상세한 분자 메커니즘을 밝혀낼 수 있었다.
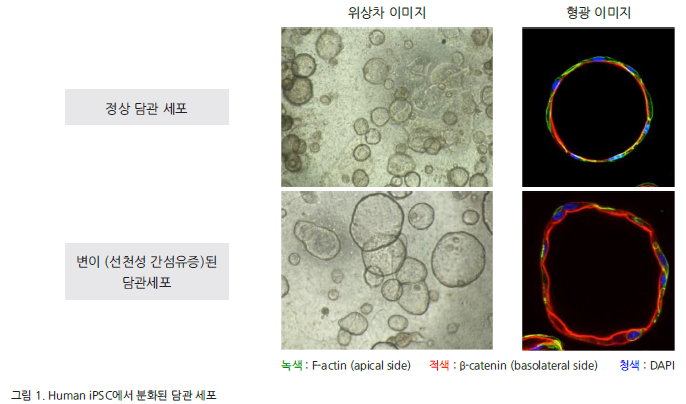
Human iPSC를 DEF-CS™ 500 Culture System에서 유지 및 배양 후, Cellartis
® iPS Cell to Hepatocyte Differentiation System을 사용하여 Hepatoblast stage까지 분화 유도했다.
분화 유도 12일째, 유도된 세포를 배양하여 간 전구 세포 (iPS-HPCs) colony를 형성시켰고, 이 세포를 3D 배양으로 10일 동안 추가 배양하면 담관 상피로 구성된 낭(Cyst)형태로 분화되었다.
선천성 간섬유증 모델의 변이 세포는 자율적으로 IL-8을 분비하고, 분비된 IL-8에 의존적으로 담관 세포가 증식하여 Cyst의 크기와 수가 증대하는 것을 확인하였다. 이러한 현상은
태아기의 담관 형성 이상으로 인한 질환을 모방하고 있는 것으로 생각된다.
(Tsunoda, et al.,Journal of Hepatology (2019) 인용)
https://doi.org/10.1016/j.jhep.2019.02.024

 |
Cellartis® iPS Cell to Hepatocyte Differentiation System을 어떻게 사용하게 되셨나요?
- 제품을 사용하고있는 공동 연구자로부터 안정적으로 배양이 가능하다고 들었습니다. 또한, 연구실에서
Feeder free 배양으로 변경하려는 계획이 있었기 때문에, 본 제품을 사용하게 되었습니다. |
| |
|
 |
실제로 사용해본 소감은 어떻나요?
- Feede-free 배양은 비교적 간편함과 동시에, human iPSC를 안정적으로 배양할 수 있었습니다.이 연구에서는
간 전구 세포까지 분화시킨 후 확대 배양하여
담관 세포로 분화시키는 실험을 진행하였습니다. 기존의 간세포
계열의 분화에 사용한 방법의 결과보다 전반적인 분화 유도 과정에서 안정적인 재현성을 확인하였습니다. |
| |
|
 |
아직 사용해보지 않은 분들께 한마디 부탁 드립니다.
- Human iPSC의 유지 및 배양 뿐만아니라 간 세포 계열의 분화 유도 관련 실험까지 모두, 재현성있는 실험이
가능해, human iPSC의
사용 경험이 적은 실험자라도 배양과 분화 과정을 안정적으로 진행할 수 있다고 생각합니다. |

2. hiPSC를 이용한 다낭성 간질환 (polycystic liver disease)의 in vitro model 제작
Department of Molecular Life sciences, Tokai University of Meticine
PhD. Akihide Kamiya
Tokai 의과대학 기초의학부 분자생물과학과의 Tadahide Kotani 박사 연구실에서 Cellartis® iPS Cell To Hepatocyte Differentiation System (Code Y30055)으로 간 질병 모델을 제작하였고,
그 결과가 Stem Cell Research에 게재되었습니다.
[Publication]
Kamiya, Akihide, et al. "An in vitro model of polycystic liver disease using genome-edited human inducible pluripotent stem cells." Stem cell research 32 (2018): 17-24

다낭성 간질환 (Polycystic liver disease)은 담즙관 세포로부터 유래한 낭종이 간에 대량 발생하고 거대화되면서 주변 장기들을 압박하는 등 문제를 유발하는 희귀질환이다.
담관 세포의 돌연변이로 인한 이상 증식이 원인으로 여겨지며, Protein Kinase C substrate 80K-H (PRKCSH) 등이 질병 유발 유전자로 보고되고 있지만, 인간 세포를 이용한
다낭성 간질환 실험 모델이 없어 질병 해석에 어려움이 있었다.
본 연구에서는 다음과 같이 다발성 간질환 모델을 제작하였다.
(1) Human iPSC를 간 전구 세포로 분화 유도
(2) 분화된 간 전구세포를 Extracellular matrix에 배양하여 담관낭 세포로 분화 유도
(3) 발현 Marker를 확인하여 담관낭 세포 분화 확인
(Positive marker: Cytokeratin 7, 19 / Negative marker: α-fetoprotein)
(4) CRISPR/Cas9으로 PRKCSH 유전자가 편집된 human iPSC를 제작하고, 이를 사용하여 (1)~(3)과 같은 방식으로
담관낭 세포로 분화 유도하여 In vitro 질병 모델 제작
(5) 정상 세포보다 PRKCSH 유전자가 편집된 human iPSC는 담관낭 세포로의 분화가 촉진되는 것을 확인
(6) Human iPSC와 유전자 편집 기술을 사용해 난치성 다낭성 간질환의 in vitro 모델을 구축할 수 있음을 확인
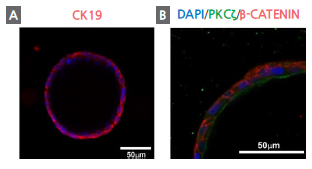
그림2. Human iPSC 유래의 간 전구세포에서 유도된 담관낭 세포의 구조
A: Human iPSC로부터 분화된 간 전구세포를 extracellular matrix gel에서 배양하였으며, 담관낭 세포의 marker인 cytokeratin 19 (CK19) 양성인 담관낭 구조를 확인하였다.
B: 유도된 담관낭 세포는 상피 조직의 극성 (basal side (β-catenin), apical side (PKCζ))을 유지하였다.
(Kamiya et al., Stem Cell Research (2018) 인용)
https://www.sciencedirect.com/science/article/pii/1873506118302113

 |
Cellartis® iPS Cell to Hepatocyte Differentiation System을 어떻게 사용하게 되셨나요?
많은 연구자들이 이미 human iPSC로부터 다양한 간세포 분화 방법을 보고하고 있으며, 우리 또한 연구 중입니다.
Feeder cell을 사용할 경우, feeder cell로 인해 iPSC의
간세포 분화 유도가 불안정해 질 수 있기 때문에 Feeder-free로
iPSC의 배양이 가능한 Cellartis system을 사용하기로 결정하였습니다. |
| |
|
 |
실제로 사용해본 소감은 어떻나요?
Feeder cell을 사용해서 배양했을 때 보다 Cellartis의 iPSC feeder-free culture 배지 (Cellartis® DEF-CS™ 500 Culture
System (Code Y30010))와 간세포 분화시스템을
사용하였을 때 매우 간편하게 줄기세포를 배양을 할 수 있었고,
human iPSC를 매우 안정적으로 간세포로 분화시킬 수 있어,
실험 효율이 현저하게 증가했습니다. |
| |
|
 |
아직 사용해보지 않은 분들께 한마디 부탁 드립니다.
Human iPSC를 간세포로 분화하는 과정에서는 일반적으로 세포 밀도 등에 의해 분화 효율과 실험 결과가 크게
달라질 수 있습니다. Cellartis 시스템은 재현성이 높은 안정적인 결과를
제공하기 때문에, 실험 효율을 증가시키고자
하는 연구자에게 추천합니다. |
본 후기는 일문 인터뷰 내용의 번역본으로, 원문은 http://www.takara-bio.co.jp 에서 확인할 수 있습니다.


iPSC Derived Hepatocyte
Human iPSC/ESC로부터 고순도 Hepatocyte로 분화
Cellartis® iPS Cell to Hepatocyte
Differentiation System (Code Y30055)
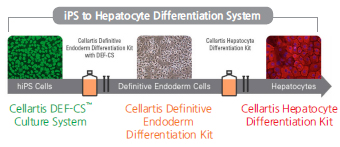
- 25개 이상 줄기세포주에서 90% 이상 고순도 간세포 분화 확인
- 단계별 분화 진행, protocol 최적화 과정 불필요
- 높은 재현성으로 안정적인 실험 결과
- All-in-One Kit로 분화에 필요한 모든 제품 포함
Primary Hepatocyte
Human primary hepatocyte 배양을 위한 선택
Cellartis® Power™ Primary HEP Medium
(Code Y20020)
- 다양한 제조사의 Hepatocyte 장기 배양 가능 (4주)
- 약물대사, 약물유도기능 등 각종 metabolism 측정 가능
- 격일 배지 교환 (Weekend Free), 번거로운 overlay 불필요
- 다양한 Application 적용 : 장기 간독성 시험, HBV, HCV,Intrinsic clearance 등
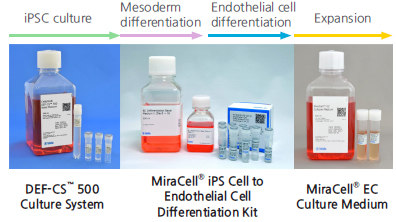
혈관 내피 세포 (Vascular Endothelial Cells)의 질병 모델 개발을 위한 Solution
MiraCell® iPS Cell to Endothelial Cell Differentiation Kit (Code Y50300)
- 보유 중인 human iPSC로부터 혈관내피세포로 분화 유도
- 최적화 과정 없이 높은 분화 효율 (>80%) 확인
- 분화 유도된 혈관내피세포는 동결 보존 및 확대 배양 가능