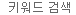- 고객지원
- 업무안내│제품문의
- 전화번호│02-2081-2510
- Email │support@takara.co.kr
- 대전지사
- 업무안내│대전/충청지역 주문, 제품문의
- 전화번호│042-828-6525
- Email │tkbd@takara.co.kr
- 업무시간안내
- [ 평 일 ] 09 : 00 ~ 18 : 00 │ [ 점심시간 ] 12 : 00 ~ 13 : 00
- 토·일요일, 공휴일은 휴무입니다.
[Cancer Research] Immunotherapy


CAR T-cell therapy: the latest weapon in the fight against cancer
암은 가장 오래되고 치명적인 질병으로, 3,500년 전 이집트의 의학 서적인 Edwin Smith Papyrus에서 처음 소개되었으나 아직까지 치료법이 개발되지 않았다. 수천년 동안 암세포를 표적 제거하기 위해 외과적 수술, 방사능 치료, 화학 요법을 진행하여 효과를 확인하였으나, 결과적으로 상당한 신체 손상이 유발되고 암 유형에 따라서도 그 치료 효과가 다르게 나타났다. 이러한 치료 이후에도 암이 지속되거나 암이 재발하는 경우에는 예후 또한 좋지 않았다.
백혈병이나 림프종과 같은 혈액암이 발생하면 백혈구가 통제 불가능할 정도로 분열하고, 골수나 림프절에서 다른 혈액 세포들은 밀려나오게 된다. 일반적으로는 빠르게 분열하는 암세포를 표적으로 사멸하는 세포 독성 약물을 이용한 림프구 제거 화학요법 (lymphodepletion chemotherapy)을 1차 치료로 진행한다. 그러나 이 치료법은 암세포 뿐 아니라 조혈모세포 (blood-forming hematopoietic stem cells, HSCs)나 모낭 및 위장관 세포 등에도 영향을 미쳐, 탈모나 메스꺼움, 인지/기억 장애, 감각 변화 (특히 후각, 미각), 면역 체계의 이상이 발생할 수 있으며 생명에 치명적인 위협을 유발할 수 있다. 1차 치료가 성공적으로 진행되면 환자는 적절한 공여자로부터 HSC를 이식 받음으로써 완치될 수 있으나, 이식된 면역세포의 거부반응으로 이식 편대 숙주병(Graft versus host disease, GVHD)과 같은 합병증이 발생할 수 있다.
최근 연구되는 CAR-T 치료 (Chimeric antigen receptor T-cell therapy)라는 신기술은 혈액암 환자의 T 세포가 암세포를 공격하게 만듦으로써, 조혈모세포 이식이나 반복적인 화학 요법으로 인한 부작용 없이도 암을 치료할 수 있을 것으로 보인다. 다카라바이오는 CAR-T 세포 치료를 성공적으로 연구할 수 있도록 다양한 제품을 지원하고 있다.
Weaponizing the patient’s immune system
기존의 항암제를 이용한 치료법과 달리, CAR-T 치료법의 강점은 T 세포 자체의 방어 기전을 이용하는 것에 있다. 일반적인 면역 반응에서 감염된 숙주 세포는 조직 적합성 복합체 (Major Histocompatibility Complex, MHC)를 이용해 세포 표면에 외인성 항원을 나타낸다. T 세포는 특정 TCR (T-cell Receptor)를 이용해 MHC/항원 복합체에 결합하여, 세포가 나타내는 항원이 내인성인지 외인성인지를 판별한다. 내인성 항원의 경우 T 세포에서 면역반응이 일어나지 않으나, 외인성 항원을 인식하는 경우 T 세포가 세포 독성 매개체를 감염 세포에 직접 전달하여 세포 사멸을 유발한다.
이 면역 반응이 암과 어떻게 관련되어 있는지 살펴 보면, 급성 림프구성 백혈병 (Acute Lymphocytic Leukemia, ALL)이나 거대 B 세포 림프종 (Diffuse Large B-Cell Lymphoma, DBLCL)과 같은 B 세포 암의 경우, 유전적 및 후성적 변화로 인해 정상 B 세포가 암세포로 변화하게 된다. T 세포는 이렇게 변형된 단일 B 세포의 항원 수용체 일부를 인식하여 종양 특이적 항원으로 인식한다. CD19는 B 세포에서 특이적으로 발현하는 signal 단백질로써 악성 B 세포에서 높게 발현하고, 조혈모 줄기세포에서 낮은 발현을 보이기 때문에, 이를 타겟하도록 T 세포를 조작하면 중요한 조혈모세포의 손상 없이 치료가 가능하다.
CAR-T 세포는 이 작용 기전을 이용하여, 특히 악성세포를 사멸하도록 조작되며, 1) CD19와 같은 특정 암 항원을 인식하거나 2) TCR에서 보이는 세포 독성 성분을 결합하여 제작된다. CAR-T 치료법은 암 항원을 인식할 수 있도록 림프구에 TCR 유전자를 도입하고, 림프구 제거 화학요법을 진행한 환자에게 다시 주입함으로써 새로운 림프구가 암 세포를 인식하게 하고, 면역반응을 통해 제거하는 과정으로 진행된다 (그림 1).
만성 림프구성 백혈병 (Chronic Lymphocytic Leukemia, CLL) 환자를 대상으로 한 연구에서 CAR-T 치료법은 기존의 조혈모세포 이식 치료법에 비해 몇몇 장점을 가진다. 실제 환자의 세포를 그대로 이용했기 때문에 GVHD로 인한 부작용을 방지할 수 있었을 뿐 아니라, CAR-T 세포를 4배로 확대 배양할 수 있었고, 6개월 이상 세포가 유지되는 장점을 볼 수 있었다 (Kalos 2016). 이 연구를 통해 몇몇 환자들은 완치되었으나 일부 부작용도 확인되었다.
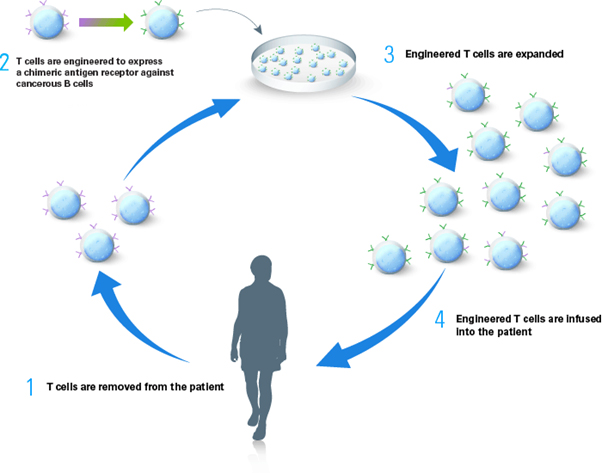
그림 1. T-cell을 이용한 치료 과정
CAR T-cell therapy involves removing a leukemia or lymphoma patient's T cells by leukapheresis (Step 1), modifying and expanding the T cells ex vivo so they express a chimeric antigen receptor that recognizes cancerous B cells (Steps 2 and 3), and then reinfusing the CAR T cells back into the same patient (Step 4). Several commercially available products (encompassing the aforementioned process) take the autologous approach (cells come from and are infused back into the same patient, avoiding GVHD), while several companies are developing therapies that use Steps 1-3 of the workflow but can be used to treat thousands of patients (allogeneic approach).
CAR T-cell therapies on the battlefield
현재, B 세포 암이 재발하거나 화학 요법에 내성이 있던 몇몇 환자에서는 두 종류의 CAR-T 치료법이 적용되고 있다. KTE-C19 / axicabtagene ciloleucel (axi-cel)은 DLBCL 치료를 위해 처음으로 2017년에 FDA 승인을 받은 CAR T 세포 치료제다. 2018년 5월에도 재발성/불응성의 DLBCL 뿐만 아니라 재생성/불응성의 B 세포 전구체 ALL의 치료에 적용 가능한 tisagenlecleucel이 FDA 승인을 받았다. 놀랍게도 임상 2상에서 tisagenlecleucel로 치료한 ALL 환자 53명 중 83%가 완치되었다. 또한 DLBCL 환자 81명 중 53%는 완치되었으며, 완치된 환자의 74%는 6개월 후에도 암이 재발되지 않았다 (Ogba et al. 2018).
이렇게 좋은 결과가 있었음에도 불구하고, 아직 CAR T 세포 치료제는 부작용을 동반한다. 사이토카인 방출 증후군 (Cytokine release syndrome, CRS)은 열, 식욕 부진, 통증과 같은 증상을 동반하며, 빠른 심박동이나 발작, 저혈압, 호흡 곤란 등 생명을 위협할 수도 있다 (Brudno and Kochenderfer 2016). 이 치료법은 뇌병증, 발작, 떨림과 같은 신경학적 합병증이 발생될 수 있지만 대부분 가역적이었다.
The future of cancer warfare
그럼에도 불구하고 CAR T 세포 치료제는 무한한 가능성을 가지고 있어, 연구자들은 CAR T 세포 치료제 기술을 발전시켜 부작용이나 off-target 효과를 최소화하는 방법 (reviewed in Bonifant et al. 2016) 외에도 표적 세포의 독성과 사이토카인 생산, T 세포 증식 및 생존을 개선하고 있다 (그림 2). 게다가 현재 FDA에서 승인된 치료법이 CD19를 타겟으로 하는 반면, CD20, CD22, CD23, ROR1 등과 같이 다른 B 세포 항원을 타겟으로 하는 치료제의 임상 테스트도 진행 중에 있다 (D’Aloia et al. 2018).
그림 2. CAR T 세포 구조의 진화
Building on the original CAR T-cell technology, later generations have incorporated additional elements to aid in T-cell persistence, proliferation, cytokine production, and survival. Fourth-generation CAR T cells (termed "armored CARs") use modified second-generation CAR T cells engineered to express and secrete cytokines to improve efficacy. Image: Monica Casucci and Attilio Bondanza / Public Domain.
[원문] CAR T-cell therapy: the latest weapon in the fight against cancer
[참고문헌]
- Adusumilli, P. S. et al. ASGCT 2018 presentation: A Phase I Clinical Trial of Malignant Pleural Disease Treated with Regionally Delivered Autologous Mesothelin-Targeted CAR T Cells: Safety and Efficacy - A Preliminary Report.
- Bonifant, C. L., Jackson, H. J., Brentjens, R. J. & Curran, K. J. Toxicity and management in CAR T-cell therapy. Mol. Ther. - Oncolytics 3, 16011 (2016).
- Brown, C. E. et al. Bioactivity and Safety of IL13R 2-Redirected Chimeric Antigen Receptor CD8+ T Cells in Patients with Recurrent Glioblastoma. Clin. Cancer Res. 21, 4062-4072 (2015).
- Brown, C. E. et al. Regression of Glioblastoma after Chimeric Antigen Receptor T-Cell Therapy. N. Engl. J. Med. 375, 2561-2569 (2016).
- Brudno, J. N. & Kochenderfer, J. N. Toxicities of chimeric antigen receptor T cells: recognition and management. Blood 127, 3321-30 (2016).
- D'Aloia, M. M., Zizzari, I. G., Sacchetti, B., Pierelli, L. & Alimandi, M. CAR-T cells: the long and winding road to solid tumors. Cell Death Dis. 9, 282 (2018).
- Kalos, M. Chimeric antigen receptor-engineered T cells in CLL: the next chapter unfolds. J. Immunother. Cancer 4, 5 (2016).
- Ogba, N. et al. Chimeric Antigen Receptor T-Cell Therapy. J. Natl. Compr. Canc. Netw. 16, 1092-1106 (2018).
암은 가장 오래되고 치명적인 질병으로, 3,500년 전 이집트의 의학 서적인 Edwin Smith Papyrus에서 처음 소개되었으나 아직까지 치료법이 개발되지 않았다. 수천년 동안 암세포를 표적 제거하기 위해 외과적 수술, 방사능 치료, 화학 요법을 진행하여 효과를 확인하였으나, 결과적으로 상당한 신체 손상이 유발되고 암 유형에 따라서도 그 치료 효과가 다르게 나타났다. 이러한 치료 이후에도 암이 지속되거나 암이 재발하는 경우에는 예후 또한 좋지 않았다.
백혈병이나 림프종과 같은 혈액암이 발생하면 백혈구가 통제 불가능할 정도로 분열하고, 골수나 림프절에서 다른 혈액 세포들은 밀려나오게 된다. 일반적으로는 빠르게 분열하는 암세포를 표적으로 사멸하는 세포 독성 약물을 이용한 림프구 제거 화학요법 (lymphodepletion chemotherapy)을 1차 치료로 진행한다. 그러나 이 치료법은 암세포 뿐 아니라 조혈모세포 (blood-forming hematopoietic stem cells, HSCs)나 모낭 및 위장관 세포 등에도 영향을 미쳐, 탈모나 메스꺼움, 인지/기억 장애, 감각 변화 (특히 후각, 미각), 면역 체계의 이상이 발생할 수 있으며 생명에 치명적인 위협을 유발할 수 있다. 1차 치료가 성공적으로 진행되면 환자는 적절한 공여자로부터 HSC를 이식 받음으로써 완치될 수 있으나, 이식된 면역세포의 거부반응으로 이식 편대 숙주병(Graft versus host disease, GVHD)과 같은 합병증이 발생할 수 있다.
최근 연구되는 CAR-T 치료 (Chimeric antigen receptor T-cell therapy)라는 신기술은 혈액암 환자의 T 세포가 암세포를 공격하게 만듦으로써, 조혈모세포 이식이나 반복적인 화학 요법으로 인한 부작용 없이도 암을 치료할 수 있을 것으로 보인다. 다카라바이오는 CAR-T 세포 치료를 성공적으로 연구할 수 있도록 다양한 제품을 지원하고 있다.
Weaponizing the patient’s immune system
기존의 항암제를 이용한 치료법과 달리, CAR-T 치료법의 강점은 T 세포 자체의 방어 기전을 이용하는 것에 있다. 일반적인 면역 반응에서 감염된 숙주 세포는 조직 적합성 복합체 (Major Histocompatibility Complex, MHC)를 이용해 세포 표면에 외인성 항원을 나타낸다. T 세포는 특정 TCR (T-cell Receptor)를 이용해 MHC/항원 복합체에 결합하여, 세포가 나타내는 항원이 내인성인지 외인성인지를 판별한다. 내인성 항원의 경우 T 세포에서 면역반응이 일어나지 않으나, 외인성 항원을 인식하는 경우 T 세포가 세포 독성 매개체를 감염 세포에 직접 전달하여 세포 사멸을 유발한다.
이 면역 반응이 암과 어떻게 관련되어 있는지 살펴 보면, 급성 림프구성 백혈병 (Acute Lymphocytic Leukemia, ALL)이나 거대 B 세포 림프종 (Diffuse Large B-Cell Lymphoma, DBLCL)과 같은 B 세포 암의 경우, 유전적 및 후성적 변화로 인해 정상 B 세포가 암세포로 변화하게 된다. T 세포는 이렇게 변형된 단일 B 세포의 항원 수용체 일부를 인식하여 종양 특이적 항원으로 인식한다. CD19는 B 세포에서 특이적으로 발현하는 signal 단백질로써 악성 B 세포에서 높게 발현하고, 조혈모 줄기세포에서 낮은 발현을 보이기 때문에, 이를 타겟하도록 T 세포를 조작하면 중요한 조혈모세포의 손상 없이 치료가 가능하다.
CAR-T 세포는 이 작용 기전을 이용하여, 특히 악성세포를 사멸하도록 조작되며, 1) CD19와 같은 특정 암 항원을 인식하거나 2) TCR에서 보이는 세포 독성 성분을 결합하여 제작된다. CAR-T 치료법은 암 항원을 인식할 수 있도록 림프구에 TCR 유전자를 도입하고, 림프구 제거 화학요법을 진행한 환자에게 다시 주입함으로써 새로운 림프구가 암 세포를 인식하게 하고, 면역반응을 통해 제거하는 과정으로 진행된다 (그림 1).
만성 림프구성 백혈병 (Chronic Lymphocytic Leukemia, CLL) 환자를 대상으로 한 연구에서 CAR-T 치료법은 기존의 조혈모세포 이식 치료법에 비해 몇몇 장점을 가진다. 실제 환자의 세포를 그대로 이용했기 때문에 GVHD로 인한 부작용을 방지할 수 있었을 뿐 아니라, CAR-T 세포를 4배로 확대 배양할 수 있었고, 6개월 이상 세포가 유지되는 장점을 볼 수 있었다 (Kalos 2016). 이 연구를 통해 몇몇 환자들은 완치되었으나 일부 부작용도 확인되었다.

그림 1. T-cell을 이용한 치료 과정
CAR T-cell therapy involves removing a leukemia or lymphoma patient's T cells by leukapheresis (Step 1), modifying and expanding the T cells ex vivo so they express a chimeric antigen receptor that recognizes cancerous B cells (Steps 2 and 3), and then reinfusing the CAR T cells back into the same patient (Step 4). Several commercially available products (encompassing the aforementioned process) take the autologous approach (cells come from and are infused back into the same patient, avoiding GVHD), while several companies are developing therapies that use Steps 1-3 of the workflow but can be used to treat thousands of patients (allogeneic approach).
CAR T-cell therapies on the battlefield
현재, B 세포 암이 재발하거나 화학 요법에 내성이 있던 몇몇 환자에서는 두 종류의 CAR-T 치료법이 적용되고 있다. KTE-C19 / axicabtagene ciloleucel (axi-cel)은 DLBCL 치료를 위해 처음으로 2017년에 FDA 승인을 받은 CAR T 세포 치료제다. 2018년 5월에도 재발성/불응성의 DLBCL 뿐만 아니라 재생성/불응성의 B 세포 전구체 ALL의 치료에 적용 가능한 tisagenlecleucel이 FDA 승인을 받았다. 놀랍게도 임상 2상에서 tisagenlecleucel로 치료한 ALL 환자 53명 중 83%가 완치되었다. 또한 DLBCL 환자 81명 중 53%는 완치되었으며, 완치된 환자의 74%는 6개월 후에도 암이 재발되지 않았다 (Ogba et al. 2018).
이렇게 좋은 결과가 있었음에도 불구하고, 아직 CAR T 세포 치료제는 부작용을 동반한다. 사이토카인 방출 증후군 (Cytokine release syndrome, CRS)은 열, 식욕 부진, 통증과 같은 증상을 동반하며, 빠른 심박동이나 발작, 저혈압, 호흡 곤란 등 생명을 위협할 수도 있다 (Brudno and Kochenderfer 2016). 이 치료법은 뇌병증, 발작, 떨림과 같은 신경학적 합병증이 발생될 수 있지만 대부분 가역적이었다.
The future of cancer warfare
그럼에도 불구하고 CAR T 세포 치료제는 무한한 가능성을 가지고 있어, 연구자들은 CAR T 세포 치료제 기술을 발전시켜 부작용이나 off-target 효과를 최소화하는 방법 (reviewed in Bonifant et al. 2016) 외에도 표적 세포의 독성과 사이토카인 생산, T 세포 증식 및 생존을 개선하고 있다 (그림 2). 게다가 현재 FDA에서 승인된 치료법이 CD19를 타겟으로 하는 반면, CD20, CD22, CD23, ROR1 등과 같이 다른 B 세포 항원을 타겟으로 하는 치료제의 임상 테스트도 진행 중에 있다 (D’Aloia et al. 2018).

그림 2. CAR T 세포 구조의 진화
Building on the original CAR T-cell technology, later generations have incorporated additional elements to aid in T-cell persistence, proliferation, cytokine production, and survival. Fourth-generation CAR T cells (termed "armored CARs") use modified second-generation CAR T cells engineered to express and secrete cytokines to improve efficacy. Image: Monica Casucci and Attilio Bondanza / Public Domain.
Code |
제품명 |
용량 |
T210 |
1.0 ㎎/1.0 ㎖ |
|
WK552 |
1,000 ㎖ |
|
T202 |
RetroNectin® GMP grade (Recombinant Human Fibronectin Fragment CH-296) |
2.5 ㎎/2.5 ㎖ |
FU0010 |
10 pcs |
[원문] CAR T-cell therapy: the latest weapon in the fight against cancer
[참고문헌]
- Adusumilli, P. S. et al. ASGCT 2018 presentation: A Phase I Clinical Trial of Malignant Pleural Disease Treated with Regionally Delivered Autologous Mesothelin-Targeted CAR T Cells: Safety and Efficacy - A Preliminary Report.
- Bonifant, C. L., Jackson, H. J., Brentjens, R. J. & Curran, K. J. Toxicity and management in CAR T-cell therapy. Mol. Ther. - Oncolytics 3, 16011 (2016).
- Brown, C. E. et al. Bioactivity and Safety of IL13R 2-Redirected Chimeric Antigen Receptor CD8+ T Cells in Patients with Recurrent Glioblastoma. Clin. Cancer Res. 21, 4062-4072 (2015).
- Brown, C. E. et al. Regression of Glioblastoma after Chimeric Antigen Receptor T-Cell Therapy. N. Engl. J. Med. 375, 2561-2569 (2016).
- Brudno, J. N. & Kochenderfer, J. N. Toxicities of chimeric antigen receptor T cells: recognition and management. Blood 127, 3321-30 (2016).
- D'Aloia, M. M., Zizzari, I. G., Sacchetti, B., Pierelli, L. & Alimandi, M. CAR-T cells: the long and winding road to solid tumors. Cell Death Dis. 9, 282 (2018).
- Kalos, M. Chimeric antigen receptor-engineered T cells in CLL: the next chapter unfolds. J. Immunother. Cancer 4, 5 (2016).
- Ogba, N. et al. Chimeric Antigen Receptor T-Cell Therapy. J. Natl. Compr. Canc. Netw. 16, 1092-1106 (2018).