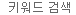- 고객지원
- 업무안내│제품문의
- 전화번호│02-2081-2510
- Email │support@takara.co.kr
- 대전지사
- 업무안내│대전/충청지역 주문, 제품문의
- 전화번호│042-828-6525
- Email │tkbd@takara.co.kr
- 업무시간안내
- [ 평 일 ] 09 : 00 ~ 18 : 00 │ [ 점심시간 ] 12 : 00 ~ 13 : 00
- 토·일요일, 공휴일은 휴무입니다.
[Cancer Research] Immunotherapy


A faster path to analysis for monoclonal antibodies as therapeutic agents
단클론항체 (Monoclonal antibodies, mAbs) 치료제는 여러 질환 중에서도 암이나 퇴행성 질환의 표적 치료에 사용되고 있다. 이 치료제는 표적 세포로의 높은 특이성이나 활성, 약물동태학 (Pharmacokinetics, PK) 측면에서 높은 가능성을 보인다. 약물 개발의 초기 단계에서 PK 연구는 bioavailability, 제거 효율, 반감기, metabolic profile과 같은 매개 변수를 평가하는 지표로 사용되고 있다. 이 분야에 대한 관심도가 증가함에 따라, 항체의 생산이나 정제 과정을 간소화하여 분석 과정을 보다 빠르게 진행할 수 있는 방법이 요구되고 있다.
액체 크로마토그래피를 이용한 질량 분석법 (LC-MS/MS)은 후보 약물의 평가를 위해 단백질 특성 분석과 정량에 가장 많이 사용되는 기술이다 (Robinson et al. 2020). 최근, Merck & Co. Inc. 연구원들은 다카라바이오의 과학자들과 협력하여 LS-MS/MS 분석을 위한 단백질 처리 과정에 사용되는 다양한 방법을 검토하였다. 기존에는 Immunoaffinity purification (IP)나 효소를 이용해 LC-MS/MS 샘플을 준비하는 방법이 주로 사용되었으나 상당한 시간이 요구된다는 한계가 있었다. Robinson et al. 에서는 이의 대안으로 membrane 기반의 고유 기술을 적용함으로써 시간을 크게 감축하였을 뿐 아니라, PK 후속 연구를 진행할 만큼 충분한 감도의 단백질을 얻었다 (그림 1). Membrane 기반의 LC-MS 분석 단백질 정제 과정은 치료제 개발 과정을 단축시키는 데 중요한 역할을 한다.
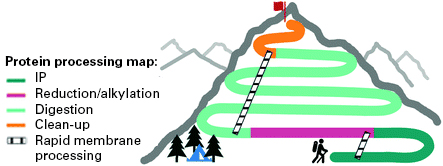
그림 1. LC-MS 기반의 분석을 위한 단백질 샘플의 처리 과정
In two key areas, IP and digestion, rapid membrane processing enables a significant cut in overall time required. Reproduced from Robinson et al. 2020 with permission from The Royal Society of Chemistry.
A question of time
연구자들은 기존의 단백질 정제 방법과 기발하고 적용성이 높은 Membrane 기반의 Capturem™ 기술을 비교하였다. 각 실험은 universal mAb standards (각 SILuLite, SILuMab)가 표지된 IgG1 λ stable isotype의 light chain과 heavy chain을 샘플로 사용했다. 전형적인 IP와 효소 처리를 이용했을 때에는 전 과정이 약 20시간 정도가 소요되었던 반면, Capturem™을 이용했을 때에는 spin column과 96 well plate 형태에서 모두 각 3~4시간 정도가 소요되었다 (그림 2). 가장 시간을 단축한 단계는 효소 처리 과정으로, 기존 단백질 정제 과정에서 가장 큰 한계점으로 여겨졌던 단계였다. 본 논문의 저자는 96 well plate의 프로토콜을 최적화해 자동화하면 더 나은 결과를 얻을 수 있을 것에 대한 기대를 내비쳤다.
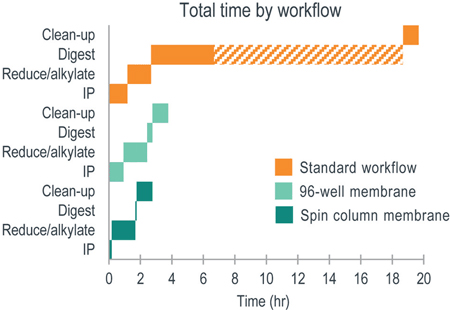
그림 2. 단백질 정제 방법에 따른 소요 시간 비교
For the standard workflow, solid areas show the 4-hour minimum of a typical nonaccelerated workflow, and the striped area shows the additional time required for overnight digestion (16 hours in total). Capturem IP reduced IP time from 70 minutes to 15 minutes for individual spin columns or 55 minutes for 96-well plates (partially automated on a liquid handler). Trypsin digestion went from 16 hours with the standard method down to just a few minutes for individual spin columns and about 20 minutes for the 96-well plates. Both systems utilized the same reduction, alkylation, and cleanup steps. Reproduced from Robinson et al. 2020 with permission from The Royal Society of Chemistry.
Evaluating the antibody digestion profile
Membrane 기반의 정제법의 성능을 정확히 평가하기 위해, 본 논문의 저자들은 trypsin column에 샘플을 연속적으로 추가로 로딩하여 분석하였다. 샘플을 한번만 로딩하여 정제했을 때, Sequence coverage가 heavy chain 83%, light chain 39%로 가장 높았던 반면, missed cleavage 또한 heavy chain 25%, light chain 39%로 가장 높았다. 추가로 샘플을 로딩하여 분석했던 샘플의 경우 이 두 지표가 모두 약간씩 감소하였으며, 총 4번의 샘플 로딩을 진행했을 때 기존에 방법보다 더 높은 수준의 Peptide digestion을 보였다. Robinson et al.은 이를 통해서 Capturem™을 이용한 방법이 기존 단백질 정제 방법에 비해 더 높은 성능을 보였음을 확인했다.
이 과정에서 Solution 방법을 이용했을 때 보였던 key peptide들도 일관적으로 확인되었으며, peptide와 항체의 식별과 정량에도 적용 가능했다. Capturem™ Trypsin으로 정제된 단백질은 sequence coverage와 cleavage 분석을 진행했을 대 PK 연구의 downstream 분석에 충분했다.
Membrane-based technology proves its value
본 논문의 저자는 96 well 형태의 Capturem™을 사용해 유방암과 위암 치료에 사용되는 단클론항체인 Hepceptin을 투여한 rat plasma 5㎕을 이용해 PK 연구를 수행하였다. 이 과정에서 GPS peptide와 TPE peptide의 확인 및 정량을 진행했으며, 결과 분석을 통해 Capturem™을 이용한 단백질 정제 과정은 간소하고 빠를 뿐 아니라 PK 분석에도 충분함을 확인하였다.
그림 3. Herceptin을 복용한 rat에서의 PK 연구 분석 결과
Five samples each were processed either by membrane-based (dark green) or standard methods (light green). Concentration results for Herceptin were based on GPSVFPLAPSSK (GPS; Panel A), and TPEVTCVVVDVSHEDPEVK (TPE; Panel B) was used for confirmation. The linear log-linear trapezoidal method was used to calculate AUC. Initial concentration (C0) was determined by linear extrapolation using the first three time points (0.25, 0.5, and 1 hr). The last three time points (24, 72, and 168 hr) were used as regression points for PK calculations. Reproduced from Robinson et al. 2020 with permission from The Royal Society of Chemistry.
An easier journey to drug discovery
연구자들이 생명을 위협하는 다양한 질병을 표적으로 하는 치료제를 개발하려면, 이를 뒷받침할 여러 실험 도구들이 중요하다. 실험 시간과 비용을 감축하는 것은 궁극적인 치료제 개발과 여러 환자들의 치료 시기를 앞당기는데 큰 차이를 만들 수 있다. 약물을 개발하는 과정은 복잡하고 까다로운 과정과 분석이 필요하지만, 단클론항체와 같은 큰 분자를 이용한 치료제가 점차 각광받고 있다. 다카라바이오는 이와 같은 항체 치료제를 위해, 높은 처리량과 간소화된 공정을 지원할 수 있는 Capturem™ 기술과 다양한 제품을 지원하고 있다.
*상기의 4종 제품은 모두 2022년 8월 종매되었습니다.
[원문] A faster path to analysis for monoclonal antibodies as therapeutic agents
[참고문헌]
- Robinson, M.R., et al., Improving the throughput of immunoaffinity purification and enzymatic digestion of therapeutic proteins using membrane-immobilized reagent technology. Analyst 145, 3,148-3,156 (2020).
단클론항체 (Monoclonal antibodies, mAbs) 치료제는 여러 질환 중에서도 암이나 퇴행성 질환의 표적 치료에 사용되고 있다. 이 치료제는 표적 세포로의 높은 특이성이나 활성, 약물동태학 (Pharmacokinetics, PK) 측면에서 높은 가능성을 보인다. 약물 개발의 초기 단계에서 PK 연구는 bioavailability, 제거 효율, 반감기, metabolic profile과 같은 매개 변수를 평가하는 지표로 사용되고 있다. 이 분야에 대한 관심도가 증가함에 따라, 항체의 생산이나 정제 과정을 간소화하여 분석 과정을 보다 빠르게 진행할 수 있는 방법이 요구되고 있다.
액체 크로마토그래피를 이용한 질량 분석법 (LC-MS/MS)은 후보 약물의 평가를 위해 단백질 특성 분석과 정량에 가장 많이 사용되는 기술이다 (Robinson et al. 2020). 최근, Merck & Co. Inc. 연구원들은 다카라바이오의 과학자들과 협력하여 LS-MS/MS 분석을 위한 단백질 처리 과정에 사용되는 다양한 방법을 검토하였다. 기존에는 Immunoaffinity purification (IP)나 효소를 이용해 LC-MS/MS 샘플을 준비하는 방법이 주로 사용되었으나 상당한 시간이 요구된다는 한계가 있었다. Robinson et al. 에서는 이의 대안으로 membrane 기반의 고유 기술을 적용함으로써 시간을 크게 감축하였을 뿐 아니라, PK 후속 연구를 진행할 만큼 충분한 감도의 단백질을 얻었다 (그림 1). Membrane 기반의 LC-MS 분석 단백질 정제 과정은 치료제 개발 과정을 단축시키는 데 중요한 역할을 한다.

그림 1. LC-MS 기반의 분석을 위한 단백질 샘플의 처리 과정
In two key areas, IP and digestion, rapid membrane processing enables a significant cut in overall time required. Reproduced from Robinson et al. 2020 with permission from The Royal Society of Chemistry.
A question of time
연구자들은 기존의 단백질 정제 방법과 기발하고 적용성이 높은 Membrane 기반의 Capturem™ 기술을 비교하였다. 각 실험은 universal mAb standards (각 SILuLite, SILuMab)가 표지된 IgG1 λ stable isotype의 light chain과 heavy chain을 샘플로 사용했다. 전형적인 IP와 효소 처리를 이용했을 때에는 전 과정이 약 20시간 정도가 소요되었던 반면, Capturem™을 이용했을 때에는 spin column과 96 well plate 형태에서 모두 각 3~4시간 정도가 소요되었다 (그림 2). 가장 시간을 단축한 단계는 효소 처리 과정으로, 기존 단백질 정제 과정에서 가장 큰 한계점으로 여겨졌던 단계였다. 본 논문의 저자는 96 well plate의 프로토콜을 최적화해 자동화하면 더 나은 결과를 얻을 수 있을 것에 대한 기대를 내비쳤다.

그림 2. 단백질 정제 방법에 따른 소요 시간 비교
For the standard workflow, solid areas show the 4-hour minimum of a typical nonaccelerated workflow, and the striped area shows the additional time required for overnight digestion (16 hours in total). Capturem IP reduced IP time from 70 minutes to 15 minutes for individual spin columns or 55 minutes for 96-well plates (partially automated on a liquid handler). Trypsin digestion went from 16 hours with the standard method down to just a few minutes for individual spin columns and about 20 minutes for the 96-well plates. Both systems utilized the same reduction, alkylation, and cleanup steps. Reproduced from Robinson et al. 2020 with permission from The Royal Society of Chemistry.
Evaluating the antibody digestion profile
Membrane 기반의 정제법의 성능을 정확히 평가하기 위해, 본 논문의 저자들은 trypsin column에 샘플을 연속적으로 추가로 로딩하여 분석하였다. 샘플을 한번만 로딩하여 정제했을 때, Sequence coverage가 heavy chain 83%, light chain 39%로 가장 높았던 반면, missed cleavage 또한 heavy chain 25%, light chain 39%로 가장 높았다. 추가로 샘플을 로딩하여 분석했던 샘플의 경우 이 두 지표가 모두 약간씩 감소하였으며, 총 4번의 샘플 로딩을 진행했을 때 기존에 방법보다 더 높은 수준의 Peptide digestion을 보였다. Robinson et al.은 이를 통해서 Capturem™을 이용한 방법이 기존 단백질 정제 방법에 비해 더 높은 성능을 보였음을 확인했다.
이 과정에서 Solution 방법을 이용했을 때 보였던 key peptide들도 일관적으로 확인되었으며, peptide와 항체의 식별과 정량에도 적용 가능했다. Capturem™ Trypsin으로 정제된 단백질은 sequence coverage와 cleavage 분석을 진행했을 대 PK 연구의 downstream 분석에 충분했다.
Membrane-based technology proves its value
본 논문의 저자는 96 well 형태의 Capturem™을 사용해 유방암과 위암 치료에 사용되는 단클론항체인 Hepceptin을 투여한 rat plasma 5㎕을 이용해 PK 연구를 수행하였다. 이 과정에서 GPS peptide와 TPE peptide의 확인 및 정량을 진행했으며, 결과 분석을 통해 Capturem™을 이용한 단백질 정제 과정은 간소하고 빠를 뿐 아니라 PK 분석에도 충분함을 확인하였다.

그림 3. Herceptin을 복용한 rat에서의 PK 연구 분석 결과
Five samples each were processed either by membrane-based (dark green) or standard methods (light green). Concentration results for Herceptin were based on GPSVFPLAPSSK (GPS; Panel A), and TPEVTCVVVDVSHEDPEVK (TPE; Panel B) was used for confirmation. The linear log-linear trapezoidal method was used to calculate AUC. Initial concentration (C0) was determined by linear extrapolation using the first three time points (0.25, 0.5, and 1 hr). The last three time points (24, 72, and 168 hr) were used as regression points for PK calculations. Reproduced from Robinson et al. 2020 with permission from The Royal Society of Chemistry.
An easier journey to drug discovery
연구자들이 생명을 위협하는 다양한 질병을 표적으로 하는 치료제를 개발하려면, 이를 뒷받침할 여러 실험 도구들이 중요하다. 실험 시간과 비용을 감축하는 것은 궁극적인 치료제 개발과 여러 환자들의 치료 시기를 앞당기는데 큰 차이를 만들 수 있다. 약물을 개발하는 과정은 복잡하고 까다로운 과정과 분석이 필요하지만, 단클론항체와 같은 큰 분자를 이용한 치료제가 점차 각광받고 있다. 다카라바이오는 이와 같은 항체 치료제를 위해, 높은 처리량과 간소화된 공정을 지원할 수 있는 Capturem™ 기술과 다양한 제품을 지원하고 있다.
Code |
제품명 |
용량 |
635743 |
Capturem™ Protein A 24-Well Plate - HC |
24 well plate |
635745 |
Capturem™ Protein G 24-Well Plate - HC |
24 well plate |
635722 |
Capturem™ Trypsin |
20 회 |
635728 |
Capturem™ Pepsin |
20 회 |
[원문] A faster path to analysis for monoclonal antibodies as therapeutic agents
[참고문헌]
- Robinson, M.R., et al., Improving the throughput of immunoaffinity purification and enzymatic digestion of therapeutic proteins using membrane-immobilized reagent technology. Analyst 145, 3,148-3,156 (2020).